¿Cómo avanzan los esfuerzos para hallar una vacuna contra la covid-19?
Validar una vacuna y obtener las licencias respectivas para su comercialización es un proceso que suele tardar años, pero un esfuerzo internacional y financiación sin precedentes podrían acelerar la etapa de pruebas y la permisología para conseguir una alternativa viable en aproximadamente 12 meses
El coronavirus acumula cinco meses desde su aparición y sigue causando estragos de todo tipo a nivel mundial, al infectar a más de 2 millones de personas y aproximarse a las 200.000 muertes.
La humanidad entera ha sumado esfuerzos en este momento crítico en un intento por solventar la situación. Y aunque expertos en el área de la salud y organismos internacionales han creado protocolos que sirven para mitigar la acelerada propagación del virus, todo apunta a que la respuesta definitiva solo puede llegar a través de una vacuna que limite la posibilidad de contraer covid-19 en todo el globo.
Aunque los laboratorios científicos más importantes del planeta están enfocados en desarrollar dicha vacuna, y los progresos han sido notorios en pocos meses de trabajo, los expertos advierten que el antiviral tardará cuando menos un año en producirse para las masas.
«Realmente no deberíamos esperar ver la vacuna al menos en 12 meses o más», advertía Margaret Harris, portavoz de la Organización Mundial de la Salud (OMS) durante una sesión en Ginebra.
Mientras cifras de infectados y muertes siguen en aumento, y se gesta una debacle económica que podría desatar una recesión sin precedentes en la historia moderna de la humanidad, una baraja de posibilidades se asoma.
El pasado jueves 16 de abril, el director de la OMS, Tedros Adhanom, confirmó que se trabaja en al menos 70 prototipos de vacunas y tres ya iniciaron su etapa de ensayos clínicos.
«Tres vacunas ya han comenzado los ensayos clínicos, más de 70 están en desarrollo. Y estamos trabajando con nuestros socios para acelerar el desarrollo, la producción y la distribución de las vacunas», declaró.
Con tantas posibilidades y una marcada intención de premura por parte de las autoridades, ¿Por qué calculan que debe esperarse al menos un año para encontrar una solución a esta catástrofe mundial? La respuesta radica en los minuciosos protocolos y reglamentos que deben seguirse para conseguir una vacuna efectiva y eficiente, que además pueda producirse para las masas.
¿Cómo se produce una vacuna?
Para entender qué es y cómo se produce una vacuna, es necesario precisar cómo actúan los virus que generan estas enfermedades de rápida propagación.
Un virus es un microorganismo simple, compuesto por un material genético recubierto de proteínas y ácidos nucleicos. Su principal característica es que penetra en células específicas y las utiliza para reproducirse, al utilizar el metabolismo de las mismas.
En el caso de este nuevo brote de coronavirus, cuya cepa concreta se denomina SARS-CoV-2, tiene la capacidad de introducirse en las células humanas y fabricar millones de réplicas en el cuerpo humano.
Las vacunas, por su parte, no son más que réplicas inofensivas de los virus, que se introducen en el cuerpo humano para que el sistema inmunológico desarrolle defensas capaces de anular al virus real en caso de que intente contagiar a la persona nuevamente.
Para lograrlo, los científicos deben estudiar el código genético del virus y buscar una forma de replicarlo sin sus efectos nocivos.
El código genético del virus fue obtenido por los científicos chinos en enero y rápidamente fue compartido en línea para que fuese de dominio público.

Fragmento del código del virus, que ha destacado como punto de partida para investigaciones en todo el mundo y el rastreo de las mutaciones del virus
A raíz de este hecho, el mundo viró su mirada al genoma del SARS-CoV-2 para dar inicio al proceso de obtención de la vacuna. Hay diferentes formas lograrlo, pero el método más utilizado en esta crisis es a través del vector recombinante.
Las vacunas recombinantes son más precisas, ya que no buscan que el cuerpo ataque a todo el genoma del virus, sino solo a los fragmentos o elementos que causan el contagio o afectan al ser humano. Para el SARS-CoV-2 se intentan anular las proteínas capaces de penetrar en las células, puesto que sin ellas el coronavirus no podría replicarse y perdería su nocividad.
Por este motivo, los tres proyectos actuales que recibieron visto bueno para pruebas con humanos intentan sintetizar la «proteína S», inyectarla a las personas y que sus sistemas inmunológicos desarrollen inmunidad contra este componente y dejen al virus sin mecanismos para invadir el organismo.
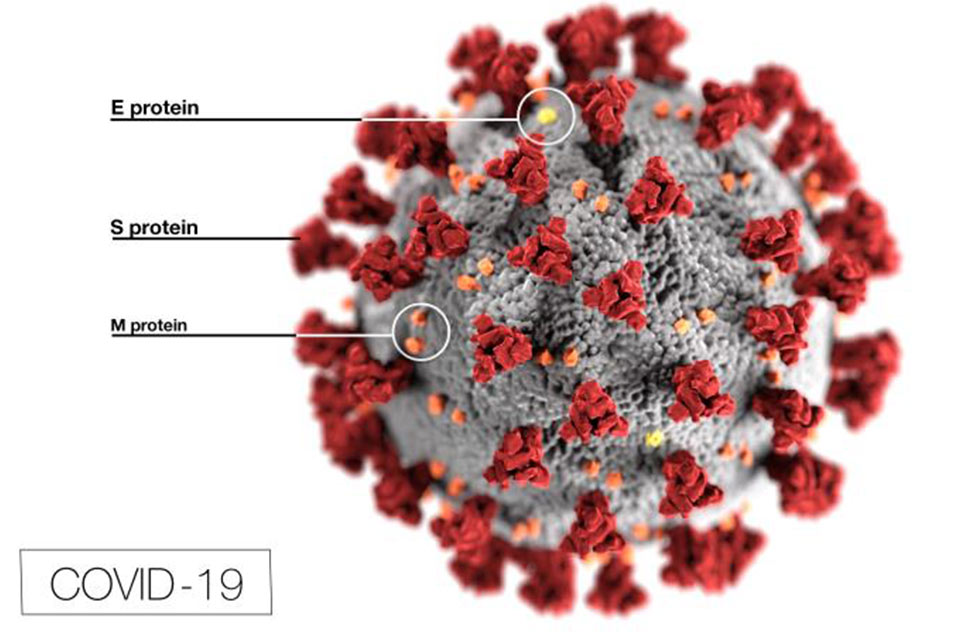
La proteína S tiene forma de puntas o «coronas». De allí surge la denominación popular del «coronavirus»
Fases de pruebas
El verdadero reto contrarreloj de esta cruzada se encuentra en la fase de pruebas con seres humanos. Validar una vacuna y obtener las licencias respectivas para su comercialización es un proceso que suele tardar años.
Cada país cuenta con sus propias regulaciones y requerimientos sanitarios para darle continuidad a estos proyectos, con plazos y condiciones distintas.
Sin embargo, el mecanismo usual para este tipo de casos establece la aplicación de tres fases de prueba en humanos, como lo indica la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) de Estados Unidos.
«Luego de completarse las pruebas de la Fase 3, y si los datos demuestran que la vacuna es segura y efectiva, entonces el patrocinador puede presentar una solicitud de licencia. A esto se le conoce como Solicitud de Licencia para Productos Biológicos (Biologics License Application, o “BLA”)», establece la FDA.
En este sentido, son dos los proyectos estadounidenses que se encuentran en proceso de pruebas en humanos. El primero lo desarrolla Moderna Therapeutics en colaboración con institutos nacionales de salud de Estados Unidos; el segundo Inovio Pharmaceuticals en colaboración con la Fundación Bill y Melinda Gates.
Ambos iniciarán con un período de pruebas en el que se administrará la vacuna a un máximo de 100 adultos sanos, mientras se les vigila para precisar posibles efectos secundarios.
Inovio anunció que 40 voluntarios se ofrecieron para participar en este proceso en dos locaciones distintas de Filadelfia.
Today we initiated Phase 1 clinical testing of our #COVID19 DNA vaccine INO-4800. Up to 40 healthy volunteers will participate at two locations. Read more about this significant step forward in the global fight against COVID-19: https://t.co/jtGyjvDPwC #DNAMedicines #DNAVaccines pic.twitter.com/ivQTEdYjOM
— INOVIO Pharmaceuticals (@InovioPharma) April 6, 2020
Sin embargo, la OMS adelanta que la vacuna experimental más avanzada es la que desarrolla la empresa china CanSino Biologics Inc junto al Instituto de Biotecnología de Beijing, puesto que se encuentra en la segunda fase de experimentos en humanos.
Ya experimentaron con 108 personas que recibieron la vacuna en tres dosis: alta, media y baja. Los pacientes que recibieron la mayor cantidad, presetaron síntomas adversos como fiebre alta y malestar en las primeras 24 horas.
La segunda fase implicará a un estimado de 500 voluntarios sanos de entre 18 y 65 años con dosis medias, bajas y también de placebo.
Ninguna propuesta ha alcanzado aún la fase tres, que implica experimentar con un grupo más grande de personas, que se determina según el caso.
Producción en masa
Otro obstáculo a superar tiene que ver con la capacidad para producir las vacunas en cantidades industriales, ya que deben distribuirse a lo largo y ancho del globo.
Algunas empresas se preparan para el momento en el que la vacuna se desarrolle y su código genético sea definido, para empezar a producirla en grandes cantidades.
Este es el caso de Johnson & Johnson que, aunque se encuentra en proceso de investigación de su propia vacuna, también se enfocan en en su capacidad de producción en aras de alcanzar una cota de 1.000 millones de dosis para distribuir.
«El mundo se enfrenta a una urgente crisis de salud pública. Estamos comprometidos a hacer nuestra parte para que la vacuna COVID-19 esté disponible y sea asequible a nivel mundial lo antes posible», dijo el presidente y director ejecutivo de la compañía, Alex Gorsky .
Las ambiciones desde China no se quedan atrás. El Grupo Farmacéutico Nacional de China (Sinopharm) ya ensaya su capacidad de producción, tras elaborar 50.000 pruebas para los ensayos clínicos iniciales. Apuntan a la elaboración de 3 millones de dosis por lote, con una cota anual de 100 millones de dosis, según reseñó la agencia de noticias estatal china, Xinhua.
Medicinas alternativas
Desde que el virus abandonó China y empezó a propagarse por todo el globo, distintas propuestas para combatir la enfermedad que genera, la covid-19, han surgido.
Debido a la premura con la que se propagó este virus nuevo, no ha dado tiempo de comprobar la efectividad de los distintos tratamientos propuestos como remedio para mitigar los efectos del virus.
Un ejemplo de los tratamientos alternativos surgidos en los últimos meses es el interferón alfa 2b humano recombinante, creado por científicos del Centro de Ingeniería Genética y Biotecnología (CIGB) de Cuba en la década de los 80.
A pesar de que el medicamento obtuvo un impacto mediático considerable, con noticias que giraron el globo afirmando que ayudó a mitigar la enfermedad en China y que es solicitado por 45 países distintos, no existe un documento científico que avale la efectividad del interferón en el combate contra el coronavirus.
Otra opción que se ha asomado es la cloroquina, un tratamiento utilizado durante años para combatir la malaria. No obstante, desató polémica porque además de que no se ha comprobado que sea eficaz contra la covid-19, provoca una serie de efectos secundarios preocupantes, como mareos, diarrea, vómitos, erupciones en la piel, entre otros.
El mundo viró brevemente su mirada hacia la ivermectina, un fármaco antiparasitario que prometía «matar» al coronavirus en el organismo en 48 horas.
Efectivamente, un estudio dirigido por el Biomedicine Discovery Institute (BDI) de la Universidad de Monash en Australia, junto al Peter Doherty Institute of Infection and Immunity (Doherty Institute), probó efectos positivos de la ivermectina en el SARS-CoV-2. Sin embargo, el cese del crecimiento del virus en el cuerpo durante su etapa de cultivo celular en 48 horas se demostró solo en un ambiente de laboratorio.
La ivermectina no se administró ni a personas ni a animales en dicho estudio, por lo que se necesitan pruebas adicionales para determinar su efectividad.
La Administración de Medicamentos y Alimentos de Estados Unidos advirtió que este fármaco solo está aprobado para consumo humano como tratamiento contra algunos gusanos parásitos, mientras que sus formulaciones tópicas solo se avalan bajo receta médica. Existen otras versiones legales solo permitidas para animales, en aras de prevenir la enfermedad del gusano del corazón y lidiar con ciertos parásitos internos y externos.
«Las personas nunca deben tomar medicamentos animales, ya que la FDA solo ha evaluado su seguridad y efectividad en las especies animales particulares para las que están etiquetados. Estos medicamentos destinados a animales pueden causar daños graves en las personas», advirtió el organismo ante el riesgo de que ciudadanos decidan automedicarse con versiones aprobadas para animales.
Un estudio publicado en el New England Journal of Medicine, basado en la observación a pacientes a los que se le aplicó el tratamiento en el hospital Jinyintan de Wuhan, determinó que el tratamiento no causa mejoras significativas en los pacientes.
El estudio incluyó a 199 pacientes de covid-19, 99 de los cuales recibieron Kaletra, mientras que al resto se le aplicó atención estándar. Después de 28 días, los investigadores concluyeron que los resultados de este medicamento no eran mejores que los obtenidos con atención estándar.
«En pacientes adultos hospitalizados con covid-19 grave, no se observó ningún beneficio con el tratamiento (de Kaletra) más allá de la atención estándar», resaltó la publicación.
Sin embargo, médicos del hospital desestimaron estos resultados y calificaron al tratamiento de «beneficioso», aunque lo descartaron como un tratamiento potencial.
La apuesta de la OMS
La OMS puso en marcha a finales de marzo el proyecto Solidaridad, un gran ensayo clínico con la participación de Argentina, Bahréin, Canadá, Francia, Irán, Noruega, Sudáfrica, España, Suiza y Tailandia. La intención es que se investigue de manera simultánea la efectividad de cuatro drogas potenciales para tratar a pacientes de covid-19.
De esta forma, se pretende recopilar la mayor cantidad de datos sobre los efectos de los fármacos en el menor tiempo posible, y ofrecer una solución parcial para neutralizar o mitigar los efectos del coronavirus en tanto se produzca la vacuna.
Según afirmó a la revista Science Ana María Henao-Restrepo, investigadora del Departamento de Vacunas y Productos Biológicos de Inmunización de la OMS, este proyecto se «está haciendo en tiempo récord».
La primera propuesta es el remdesivir, un fármaco diseñado para tratar el ébola, sin mayor éxito. Sin embargo, según pruebas preliminares de células cultivadas en laboratorios, podría tener potencial contra los coronavirus.
El segundo candidato es la ya mencionada cloroquina, que se someterá a pruebas de mayor alcance para determinar si efectivamente puede ser un arma contra la covid-19 y si sus efectos secundarios son controlables.
En tercer lugar se encuentra la combinación entre ritonavir y lopinavir, utilizada para tratar el VIH. Aunque las pruebas preliminares no son esperanzadoras, pruebas más amplias permitirán obtener conclusiones precisas.
Finalmente se ensayará una combinación entre ritonavir y lopinavir con el añadido del interferon beta -distinto al desarrollado en Cuba-.
«Será importante obtener respuestas rápidamente, para tratar de averiguar qué funciona y qué no. Creemos que la evidencia aleatoria es la mejor manera de hacerlo», concluyó Henao-Restrepo.











