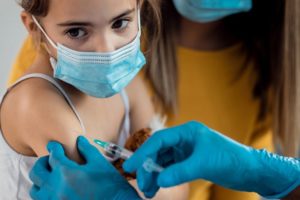
Oxford y AstraZeneca retoman ensayo de su vacuna contra el coronavirus
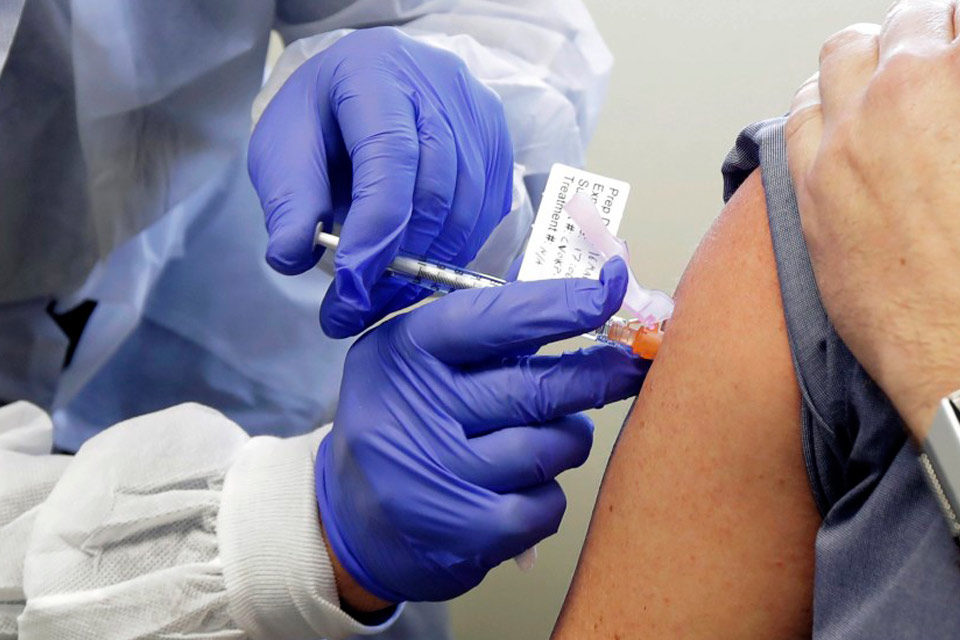
El proceso para crear esta posible vacuna contra el coronavirus se había frenado por un efecto secundario en uno de los participantes
La Universidad de Oxford ha anunciado este sábado que retoma los ensayos clínicos de su vacuna AZD1222 contra el coronavirus que ha desarrollado junto a la farmacéutica AstraZeneca, tras frenarlos el pasado viernes debido a la aparición de un efecto secundario nocivo en uno de los participantes, refiere La Vanguardia.
Los mecanismos de seguridad se activaron tras detectarse el caso. “El proceso de revisión independiente ha concluido y, siguiendo las recomendaciones tanto del comité de revisión de seguridad independiente como del regulador británico, los ensayos se reanudarán en el Reino Unido”, explica en un comunicado.
Lea también: #Especial | Cómo se ha vivido el covid-19 en Zulia
Esta posible vacuna, considerada una de las más avanzadas que se desarrollan en todo el mundo, está en las fases finales de los ensayos clínicos, antes de recibir la autorización de los organismos reguladores para proceder a inmunizar a la población.
La vacuna es la primera que debería empezar a administrarse en España. Las primeras inoculaciones estaban previstas en diciembre, según habían adelantado el ministro de Sanidad, Salvador Illa, y el presidente del Gobierno, Pedro Sánchez. La corta interrupción de los ensayos clínicos puede tener un mínimo impacto en la finalización de los estudios, su aprobación y distribución. El calendario inicial recogía tener su vacuna disponible para el primer semestre del 2021.
“A nivel mundial, unas 18.000 personas han recibido las vacunas del estudio como parte del ensayo –sobre 30.000 previstas–. En ensayos grandes como este, se espera que algunos participantes se sientan mal y cada caso debe evaluarse cuidadosamente para garantizar una evaluación cuidadosa de la seguridad”, se argumenta. De ellos, solo uno ha desarrollado una enfermedad grave, una mielitis transversa.
“Estamos comprometidos con la seguridad de nuestros participantes y con los más altos estándares de conducta en nuestros estudios y continuaremos monitoreando la seguridad atentamente”, sigue el comunicado.
AstraZeneca había iniciado la fase 3 de su ensayo en EE.UU. a finales de agosto; mientras que en el Reino Unido, Brasil y Sudáfrica, el estudio de la vacuna estaba entre las fases 2 y 3, de acuerdo a Stat. Sobre el parón en los ensayos, se expone que “el proceso de revisión estándar provocó una pausa en el estudio de la vacunación en todos nuestros ensayos globales para permitir la revisión de los datos de seguridad por un comité de revisión de seguridad independiente y los reguladores nacionales. Todas las citas de seguimiento de rutina continuaron con normalidad durante este período”.